Sumario
Situaciones clínicas
2012, vol. 5, nº 2
Importancia del diagnóstico precoz de una endocarditis bacteriana en pacientes de riesgo
Autores: Moriano Gutiérrez A1
1 Residente de cuarto año. Hospital Universitario La Fe. Programa formativo en Cardiología Pediátrica. Children´s Hospital Boston. Department of Cardiology. Harvard Medical School. Department of Pediatrics. Valencia (España).
1 Residente de cuarto año. Hospital Universitario La Fe. Programa formativo en Cardiología Pediátrica. Children´s Hospital Boston. Department of Cardiology. Harvard Medical School. Department of Pediatrics. Valencia (España).
PUNTOS CLAVE
- Es importante identificar a los pacientes con riesgo de desarrollar una endocarditis infecciosa.
- Se deben vigilar en dichos pacientes los cuadros infecciosos y tratar aquellos sugestivos de origen bacteriano, teniendo en cuenta que el tratamiento cubra a los gérmenes que habitualmente producen endocarditis bacteriana. Si la evolución del cuadro no es la esperada se debe remitir al paciente al hospital de referencia para completar el estudio.
- Se debe iniciar tratamiento antibiótico empírico en toda endocarditis clara o posible inmediatamente tras la obtención de los hemocultivos correspondientes. Hay que tener en cuenta que la mayoría de gérmenes que producen endocarditis son multirresistentes y muchos de ellos son productores de beta-lactamasas, por ello suelen utilizarse dos antibióticos con efecto sinérgico entre ellos y que sean estables frente a gérmenes productores de beta-lactamasas.
- Es necesario conocer las nuevas pautas de profilaxis de la endocarditis infecciosa: para qué pacientes está indicada, en qué situaciones y con qué tipo de antibiótico se realiza.
INTRODUCCIÓN
Los estudios realizados sobre la eficacia de la profilaxis antiendocarditis tras procedimientos invasivos son contradictorios, no son estudios prospectivos, controlados, aleatorizados y muchos solo son estudios experimentales en animales. Ninguno demuestra claramente que la reducción en duración o frecuencia de la bacteriemia lleven a una reducción en el riesgo de endocarditis y el número necesario de pacientes a tratar (NNT) es muy alto. Además se menciona el hecho de que los microtraumatismos ocasionados por el cepillado diario pueden ser también una fuente de bacteriemia, por lo que tiene mucho interés el tener una higiene dental adecuada. Por todo ello, se han modificado recientemente, las pautas sobre la profilaxis para la endocarditis infecciosa tanto en las guías europeas1 como en las americanas2,3.
Las recientes guías europeas1 de profilaxis antibiótica para la endocarditis infecciosa clasifican a los pacientes susceptibles de recibirla en pacientes de riesgo alto y pacientes de riesgo moderado (tabla 1).
Tabla 1. Mostrar/ocultar
La clasificación permite identificar a los pacientes que tienen mayor riesgo de desarrollar una endocarditis ante otro proceso infeccioso bacteriano. Así pues, actualmente la profilaxis de la endocarditis infecciosa se restringe exclusivamente a pacientes de alto riesgo y solo en los procedimientos dentales donde se manipula la encía o se perfora la mucosa oral. No obstante, las guías actuales1 sí destacan la importancia de tratar todo proceso infeccioso sospechoso de tener un origen bacteriano en pacientes de riesgo alto y moderado, vigilando que el tratamiento antibiótico utilizado cubra a los gérmenes que habitualmente ocasionan endocarditis infecciosa (tabla 2).
Tabla 2. Mostrar/ocultar
CASO CLÍNICO
Niño varón de tres años que acude a su centro de salud por cuadro de fiebre alta. Es un paciente con insuficiencia renal crónica en estadio 2 por riñón multiquístico izquierdo y nefropatía derecha secundaria a duplicidad pieloureteral con reflujo vesicoureteral grado II-III asociado. Ha padecido múltiples cuadros de pielonefritis e infecciones de orina. Presenta a su vez una cardiopatía congénita tipo canal atrioventricular de tipo transicional con comunicación interventricular muscular, comunicación interauricular tipo ostium primum y displasia valvular mitral con insuficiencia mitral ligera-moderada. Lleva tratamiento con bicarbonato, etalpha, hidropolivit y glutaferro. Hacía tres meses que se había suspendido el tratamiento antibiótico profiláctico para la infección de orina, dado que el último episodio infeccioso de origen urinario había sido hacía más de un año. Inicia cuadro febril asociado a tos seca. A la exploración solo se objetiva la orofaringe hiperémica sin exudados, taquicardia y un soplo pansistólico IV/VI conocido. Ante la sospecha de una infección respiratoria superior, se aconseja al paciente tratamiento sintomático en su domicilio.
A los tres días persiste fiebre alta, empeoramiento del estado general y a la exploración sigue resaltando el soplo y una esplenomegalia que previamente no se había constatado. Ante la sospecha de un cuadro infeccioso bacteriano sin foco claro, en un paciente de riesgo se decide remitir al paciente al hospital de referencia. Allí se efectúa analítica de sangre objetivándose una leucocitosis marcada con neutrofilia, aumento de los parámetros infecciosos, anemia, trombopenia y creatinina elevada de 1,5mg/dl (previa del paciente de 0,9 mg/dl). Se realiza un test rápido de estreptococo que resulta negativo y se toma muestra para realizar estudio de sedimento de orina y urinocultivo. El sedimento es patológico, con leucocitos, nitritos, hematíes y proteínas en la orina. Ante la sospecha de una pielonefritis aguda se ingresa al paciente, se toma un hemocultivo y se inicia tratamiento antibiótico con amoxicilina-clavulánico. Al día siguiente el niño continúa febril, mantiene la anemia, esplenomegalia, proteinuria y microhematuria. Todo ello parece explicarse por la existencia de un fenómeno de tipo inmunológico secundario al proceso infeccioso con anemia hemolítica y glomerulonefritis aguda. En el segundo día del ingreso en el hemocultivo y en el urinocultivo crece un enterococo faecalis resistente a penicilina.
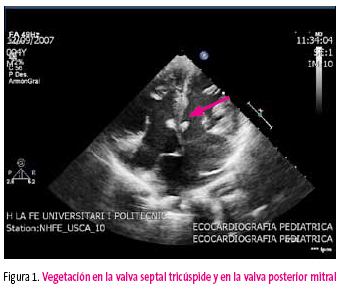
A su vez, dado el antecedente de cardiopatía congénita y la mala evolución del cuadro infeccioso, también se había solicitado una ecocardiografía con el objetivo de valorar la situación cardiológica del paciente. Es en dicha exploración donde se identifican verrugas en ambas válvulas auriculoventriculares (figura 1), diagnosticándose de endocarditis bacteriana asociada a pielonefritis aguda.
Figura 1. Mostrar/ocultar
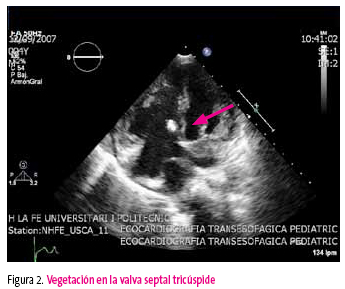
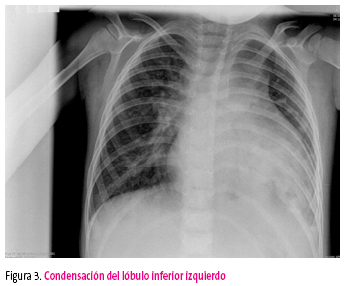
Se decide la doble terapia antibiótica siguiendo las guías europeas1 manteniéndolo durante cuatro semanas. El proceso se complica con un cuadro sospechoso de embolismo a pulmón izquierdo dada la desaparición de la parte móvil de la vegetación de la válvula mitral (figura 2) y la extensa condensación del lóbulo inferior izquierdo (figura 3).
Figura 2. Mostrar/ocultar
Figura 3. Mostrar/ocultar
Se decide actitud expectante, manteniendo el tratamiento antibiótico otras cuatro semanas más. La mejoría clínica del paciente permite el alta hospitalaria con tratamiento antibiótico oral, ciprofloxacino, al que era sensible el germen y se programa en unos meses la intervención quirúrgica para reparación de la cardiopatía estructural.
DISCUSIÓN
La endocarditis bacteriana es una complicación que puede existir en todo cuadro infeccioso sobre todo si se trata de un paciente de riesgo (tabla 1). Es importante que en dichos pacientes se traten precozmente todos los procesos infecciosos sugestivos de tener un origen bacteriano. Si la evolución del cuadro no es la esperada se debe remitir al paciente al hospital de referencia para completar el estudio. Los criterios de Duke1 (tabla 3) se utilizan para el diagnóstico de la endocarditis infecciosa, su conocimiento es muy útil cuando existe la sospecha diagnóstica para establecer, descartar o determinar el posible diagnóstico de una endocarditis infecciosa.
Tabla 3. Mostrar/ocultar
Se debe iniciar tratamiento antibiótico empírico en toda endocarditis clara o posible inmediatamente tras la obtención de los hemocultivos correspondientes. El tratamiento precoz es importante para evitar el desarrollo de una endocarditis complicada. Las guías recientes aconsejan el tratamiento inicial con amoxicilina-clavulánico más gentamicina cuando todavía no se ha aislado germen1. Se suelen utilizar dos antibióticos de entrada dado que los gérmenes suelen ser multirresistentes3 y la mayoría son productores de beta-lactamasas.
El paciente al ingreso cumplía criterios de una posible endocarditis: fiebre, fenómenos inmunológicos y ser paciente de riesgo por tener una cardiopatía congénita con lesión valvular significativa. Cuando inició el cuadro febril, a pesar de tener una exploración anodina, era un paciente de riesgo alto con el que se debería haber tenido una vigilancia más estrecha del cuadro infeccioso e iniciar el estudio del foco febril y el tratamiento más precozmente.
En niños el germen más frecuente es el Staphylococcus aureus, seguido del Streptococcus viridans y del enterococo1. El tipo de tratamiento y la duración del mismo difieren en función del germen y el tipo de válvula o material sobre el que asienta la endocarditis3. Como se ha mencionado previamente, suelen utilizarse dos antibióticos con efecto sinérgico entre ellos y siempre que sean activos frente a gérmenes productores de beta-lactamasas. Las guías aconsejan solo el tratamiento quirúrgico4 de una endocarditis en fase aguda cuando existen largas vegetaciones móviles, fenómenos embólicos repetidos, situación de inestabilidad hemodinámica o la persistencia de hemocultivos positivos a los diez días de iniciado el tratamiento correcto. En todos los demás casos se aconseja posponer la cirugía a un mes después de finalizado el tratamiento antibiótico correcto5,6.
LECTURAS RECOMENDADAS
- Guidelines on the prevention, diagnosis, and treatment of infective endocarditis. European Heart Journal. 2009;30:2369-413.
- Wilson W, Taubert KA, Gewitz M, Lockhart PB, Baddour LM, Levinson M, et al. Prevention of infective endocarditis. Circulation. 2007;116:1736-54.
BIBLIOGRAFÍA
- Guidelines on the prevention, diagnosis, and treatment of infective endocarditis. European Heart Journal. 2009;30:2369-413.
- Wilson W, Taubert KA, Gewitz M, Lockhart PB, Baddour LM, Levinson M, et al. Prevention of infective endocarditis. Circulation. 2007;116:1736-54.
- Baddour LM, Wilson WR, Bayer AS, Fowler VG, Bolger AF, Levinson ME, et al. Infective endocarditis diagnosis, antimicrobial therapy, and management of complications. Circulation. 2005;111:3167-84.
- Fariñas MC, Llinares P, Almirante B, Barberán J, de Dios Colmenero J, Garau J, et al. New trends in infective endocarditis. Enferm Infecc Microbiol Clin. 2011;29 (Supl 4):22-35.
- Byrne J, Rezai K, Sánchez JA, Bernstein RA, Okum E, Leacche M, et al. Surgical Management of endocarditis: The Society of Thoracic Surgeons Clinical Practice Guideline. Ann Thorac Surg. 2011;91:2012-9.
- Gutiérrez-Martín MA, Gálvez-Aceval J, Araji OA. Indications for Surgery and Operative Technique in Infective Endocarditis in the Present Day. Infectious Disorders-Drug Targets. 2010;10:32-46.